
ABOUT SERVICE
海外製品を、日本市場へ。
確かな橋渡し。
日本で医療機器を販売するには、
厚生労働省(PMDA)への申請・登録が必要です。
アイ・メデックスは、選任製造販売業者(DMAH)として、
海外メーカーの代理人となり、法規制対応、薬事申請、
品質保証体制の整備をサポートします。
イスラエル製マスクや台湾製デンタルミラーなどの実績をもとに、
日本市場における信頼できるパートナーとして、
多国籍企業との協働を進めています。
Strengths
規制対応を
“実務”で完結。
届出/認証の区分設計から、
JMDN/UDI、STED作成、QMS適合性調査、GVP体制構築まで一気通貫。
海外企業とPMDAの間をスムーズに橋渡しします。
-
強み #01
豊富な承認・申請実績

マスク、歯科器具など幅広い医療機器のPMDA申請をサポートしてきた実績があります。製品特性に応じた戦略的な申請スキームを提案可能です。
-
強み #02
規制対応に精通した
専門チーム
医療機器規制(薬機法・ISOなど)に精通したスタッフが在籍。海外メーカーの製品を日本市場にスムーズに導入する体制を整えています。
-
強み #03
ワンストップ支援体制

申請準備から翻訳、規制当局対応、販売後のフォローアップまで一括でサポート。取引先の負担を最小限に抑え、スピーディな市場投入を実現します。
Achievements
多国・多カテゴリ。
信頼の導入経験実績。
人工呼吸器用マスク、歯科機器等での申請・市場導入に従事。
使用目的の適正化、適合規格の洗い出し、添付文書・表示適合、
上市後安全管理(不具合報告/回収対応計画)まで運用実績があります。
-
取扱実績 #01
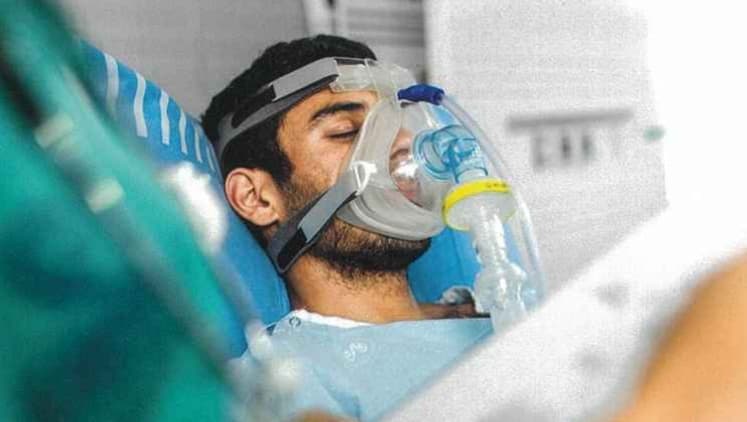
感染症対策製品の迅速導入
イスラエル製の人工呼吸器用マスクを薬機法に準拠して登録。国内緊急需要に対応し、短期間で市場投入を実現しました。
-

取扱実績 #02
歯科器具の日本市場参入支援
ドイツ製の歯科用モーターを日本市場に導入。薬事申請から販売までトータルで支援し、歯科業界における新たな選択肢を提供しました。
-

取扱実績 #03
各クラス分類への対応実績
クラスⅠの一般医療機器からクラスⅡの指定管理医療機器まで取り扱い。製品特性に応じた承認戦略の立案と実行に取り組んでいます。

海外の革新を、
この手で日本へ。
海外メーカーの革新的な医療機器を、
日本市場に確実に届けるパートナーとして、
私たちはこれまでの実績をさらに広げていきます。
国内でのノウハウを活かしながら、
将来的には日本発の技術も海外に発信し、
グローバルな医療ソリューションの橋渡しを担います。

